
인터넷이 안될 때
거지의 정체 태풍과 함께 사라진 아버지

 • 가역 반응과 비가역 반응을 설명할 수 있다.
• 가역 반응과 비가역 반응을 설명할 수 있다.
• 가역 반응에서 동적 평형을 이해하고, 비유와 예시로 설명할 수 있다.

-
석회동굴 : CaCO3(s) + CO2(g) + H2O(ℓ) ↔ Ca2+ + 2HCO3
-(aq)
-
얼음의 녹음 : H2O(s) ↔ H2O(ℓ )
-
탄산칼슘의 분해 : CaCO3(s) ↔ CaO(s) + CO2(g)

정반응과 역반응
- 화학 반응
- 정반응 : 반응들처럼 오른쪽으로 진행하는 반응 N2 + 3H2 → 2NH3
- 역반응 : 왼쪽으로 진행되는 반응 2NH3 → N2 + 3H3
- 가역 반응 : 정반응과 역반응이 모두 일어나는 반응 N2 + 3H2 ↔ 2NH3
-
가역반응에서 정반응과 역반응의 속도가 같을 때 겉으로는 반응이 멈춘 것처럼 보인다. → 화학 평형, 평형 상태
- 비가역 반응 : 한쪽으로만 진행하는 방향
- 메테인 연소 : CH4(g) + 2O2(g) → CO2(g) + 2H2O(ℓ )
- 메테인은 연소되면 이산화 탄소와 수증기가 생성된다.
- 이렇게 연소 반응으로 생성된 이산화 탄소와 수증기를 가지고 메테인을 다시 만
드는 역반응은 매우 어렵다.
- 연소 반응 이외에도 기체 생성 반응, 앙금 생성 반응, 강산과 강염기의 중화반응
등이 비가역 반응

-
우리 생활 속의 화학반응 중에서 비가역 반응을 찾아보시오.


아래의 실험 자료를 보고 온도에 따른 N2O4(g) 농도 변화를 탐구해 보자.
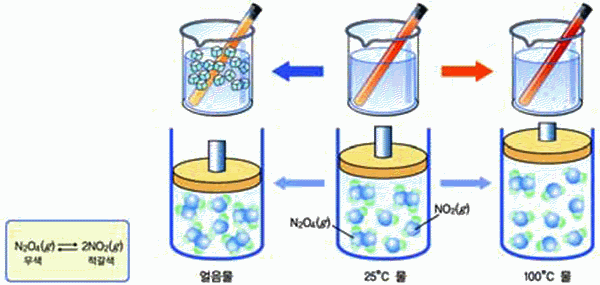
그림 Ⅲ-18 온도에 따른 N2O4(g )의 농도 변화

-
동적인 평형 상태


-
25℃로 유지가 되면 사산화 이질소(N2O4)가 생성되는 속도와 분해되는
속도가 같아지고, 두 물질의 양이 더 이상 변하지 않고 일정하게 유지되는 상태에 이른다.
-
이때는 정반응과 역반응의 속도가 같아 겉보기는 반응이 일어나지 않는 것처럼 보이며, 동적인 평형 상태를 이루게 된다.
-
화학 평형 상태
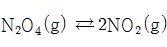
-
다음 그림은
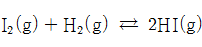
의 화학반응 속도가 동적평형 상태를 나타낼 때를 설명하는 그림이다.
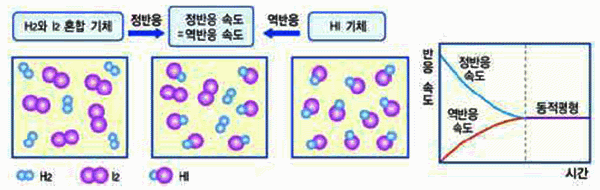
그림 Ⅲ-19 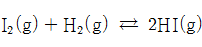 의 화학반응 속도
의 화학반응 속도

화학 평형 상태

동적 평형 상태

-
화학평형을 왜 동적평형이라고 하는가?
-
다음은
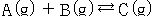
의 가역 반응을 나타낸 것이다.
-
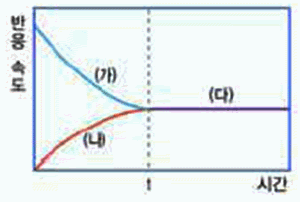
1) (가)~(다) 중 정반응 속도는?
-
2) (가)~(다) 중 C의 분해 반응속도는?
-
3) (가)~(다) 중 평형 상태를 이룬 구간은?
-
4) t시간까지는 ( )만 진행되는 것처럼 보인다. t시 간 이후에 정반응 속도와 역반응 속
도가 같으 면 A, B, C가 모두 공존한다.

인터넷이 안될 때
한 소녀의 감동 스토리(4.48)





 • 가역 반응과 비가역 반응을 설명할 수 있다.
• 가역 반응과 비가역 반응을 설명할 수 있다.





![]()


![]()

![]() 의 화학반응 속도
의 화학반응 속도

 1) (가)~(다) 중 정반응 속도는?
1) (가)~(다) 중 정반응 속도는?